对象与方法
一、研究对象
二、药物使用方法
三、观察指标
四、模拟治疗阶段量效关系
五、疗效评定
六、统计学处理
结果
一、急性ICVD患者治疗前后观察指标的变化
表1 34例急性ICVD患者治疗前后观察指标的变化( $\bar{x}±s$) |
| 检测指标 | 治疗前 | 治疗后12 h | 治疗后48 h | 治疗后72 h | F值 | P值 |
|---|---|---|---|---|---|---|
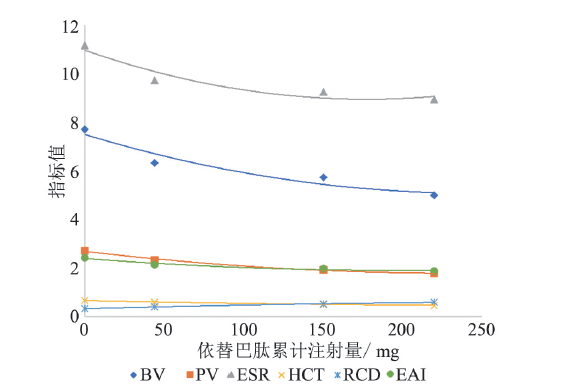
| BV/(mPa·s) | 7.72±1.32 | 6.34±0.64 | 5.73±0.72 | 5.57±0.98 | 8.657 | 0.021 |
| PV/(mPa·s) | 2.72±0.55 | 2.34±0.38 | 1.94±0.30 | 1.78±0.21 | 6.573 | 0.036 |
| ESR/(mm/h) | 11.18±5.24 | 9.75±3.92 | 9.27±3.04 | 8.97±3.54 | 9.014 | 0.019 |
| RCD | 0.32±0.09 | 0.41±0.05 | 0.52±0.04 | 0.59±0.07 | 15.205 | 0.006 |
| HCT/(L/L) | 0.67±0.05 | 0.60±0.04 | 0.51±0.02 | 0.46±0.04 | 6.458 | 0.040 |
| EAI | 2.43±0.22 | 2.14±0.19 | 1.98±0.27 | 1.89±0.32 | 6.701 | 0.037 |
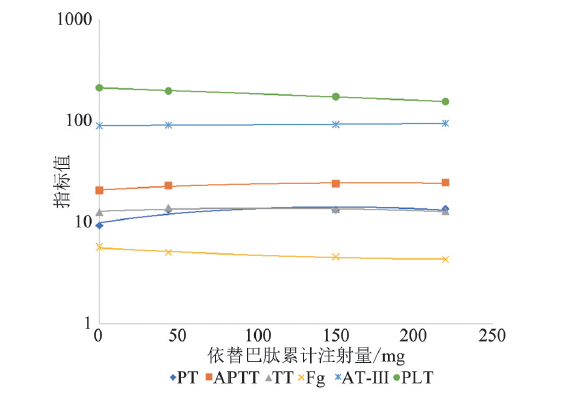
| PT/s | 9.04±1.29 | 12.88±1.35 | 13.04±1.31 | 13.26±2.06 | 9.354 | 0.017 |
| APTT/s | 20.13±4.69 | 22.66±4.88 | 23.65±4.01 | 24.03±3.85 | 6.658 | 0.038 |
| TT/s | 12.39±1.23 | 13.62±2.01 | 13.06±1.99 | 12.60±2.11 | 0.326 | 0.575 |
| Fg/(g/L) | 5.66±1.24 | 5.03±1.16 | 4.58±1.02 | 4.28±0.87 | 6.325 | 0.047 |
| AT-Ⅲ/% | 88.30±11.23 | 89.25±10.71 | 91.03±10.25 | 93.22±13.74 | 1.214 | 0.151 |
| PLT/(×109/L) | 210.23±64.12 | 195.34±54.69 | 171.48±47.88 | 153.55±49.71 | 8.324 | 0.025 |
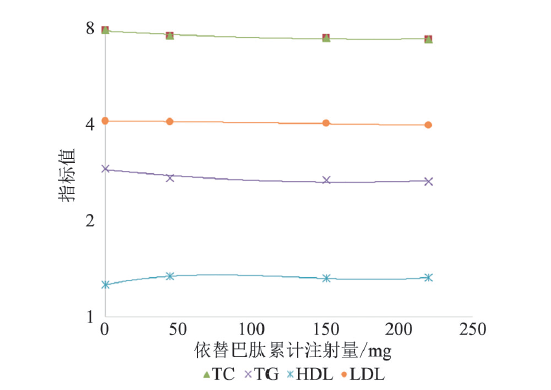
| TC/(mmol/L) | 7.92±2.38 | 7.63±2.28 | 7.49±2.21 | 7.43±2.11 | 3.439 | 0.078 |
| TG/(mmol/L) | 2.92±0.84 | 2.73±0.65 | 2.68±0.65 | 2.66±0.61 | 1.894 | 0.107 |
| HDL-C/(mmol/L) | 1.26±0.34 | 1.34±0.27 | 1.32±0.33 | 1.33±0.31 | 2.654 | 0.093 |
| LDL-C/(mmol/L) | 4.12±0.79 | 4.09±0.66 | 4.04±0.52 | 3.99±0.72 | 0.781 | 0.242 |
二、治疗阶段量效关系模拟
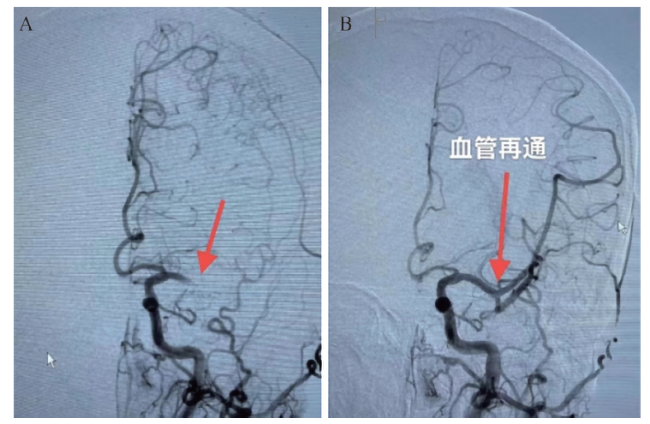
三、出血情况
四、疗效评定结果
表3 急性ICVD患者治疗前后NIHSS评分比较( $\bar{x}±s$) 单位:分 |
| 项 目 | 治疗前 | 治疗后 | Z值 | P值 |
|---|---|---|---|---|
| 男患者 | 10.67±2.37 | 4.14±1.21 | -8.325 | <0.001 |
| 女患者 | 9.89±2.19 | 4.02±1.16 | -2.753 | 0.006 |
| ACI患者 | 12.16±2.78 | 4.63±1.75 | -9.325 | <0.001 |
| TIA患者 | 9.02±1.92 | 3.85±0.89 | -7.584 | <0.001 |
| RIND患者 | 9.66±1.75 | 3.76±0.93 | -8.324 | <0.001 |
| 高血压患者 | 10.13±2.51 | 4.08±1.17 | -3.025 | 0.007 |
| 糖尿病患者 | 9.37±2.46 | 3.89±1.77 | -7.325 | <0.001 |