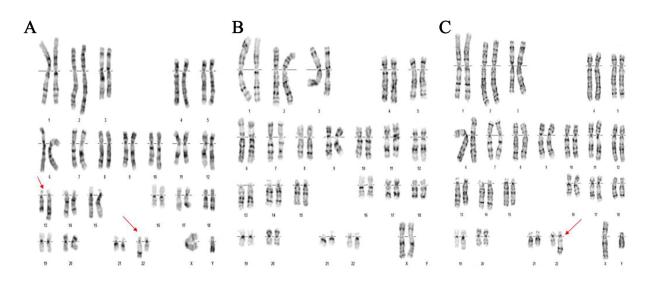
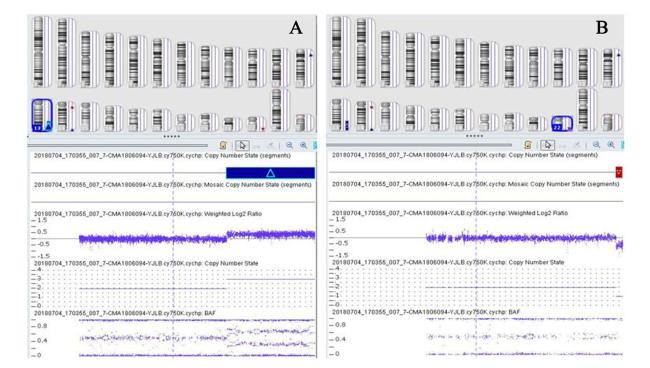
患儿男,出生7 d,系孕36
+3周自然受孕早产儿。母亲G1P1,产前未在本院规律产检,孕早期唐氏综合征筛查未见异常,停经14
+周外院彩色多普勒超声(彩超)提示胎儿大小约12
+4周,颈项透明层厚度(NT)值为2.5 mm。孕中期外院三维彩超未见明显异常。母亲36
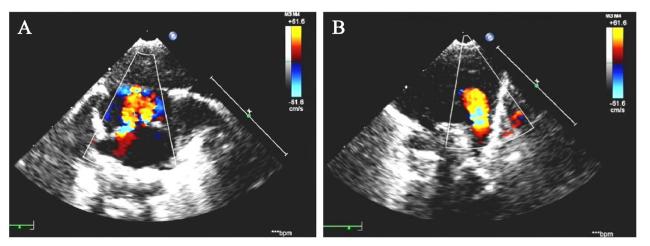
+3周外院产检发现胎心持续反应差,无下腹部疼痛,阴道无流血、流液,自觉胎动如常,予胎心监护、静脉输液治疗未见改善,遂至我院急诊就诊,拟诊胎儿宫内窘迫,行剖宫产,娩出一男性新生儿。患儿出生时体重2 850 g,身长48 cm,出生后查体反应可,前囟平软,哭声不扬,口唇微绀,双手多指畸形(六指)。辅助检查:血尿粪常规,甲状腺功能,电解质,肝功能等均正常。性激素6项:睾酮3.03 nmol/L,卵泡刺激素< 0.30 IU/L,催乳素1 431.6 mIU/L,孕酮6.89 nmol/L,黄体生成素< 0.07 IU/L,雌二醇88.02 pmol/L。彩超提示:右侧阴囊内睾丸缺如,右侧腹股沟隐睾,左侧睾丸及附睾未见明显异常;肺动脉高压(重度),动脉导管未闭,房间隔缺损(多孔,继发孔型),室间隔小缺损(肌部),三尖瓣反流(轻度),右心房右心室增大,左心室收缩功能正常,见
图1。患儿父母非近亲结婚,否认家族遗传病史,无既往病史。