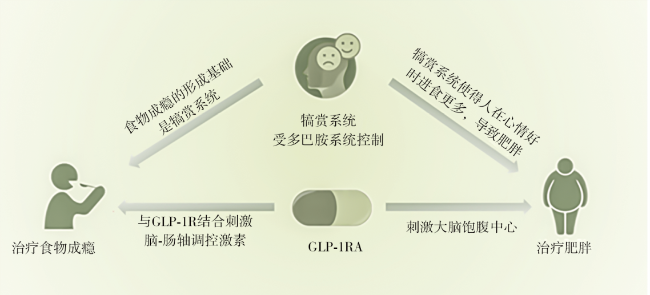
“食物成瘾是导致肥胖的根本源头”的论断让不少学者将肥胖与食物成瘾联系起来。食物成瘾的核心机制与中脑边缘多巴胺系统(mesolimbic dopamine system,MLDS)功能失调密切相关。长期高热量饮食过度激活MLDS,导致多巴胺受体敏感性下降,导致个体通过增加进食量维持快感,形成类似药物成瘾的耐受循环
[14,18]。该过程同时受乙酰胆碱对伏隔核神经元的兴奋性调控
[19]及内源性阿片系统对欣快感的强化作用
[20]驱动。值得注意的是,肠-脑轴的双向调控进一步加剧成瘾行为:肠道菌群紊乱通过迷走神经增强对高糖/高脂食物的渴求,并刺激黑质多巴胺释放以维持MLDS过度激活
[21-22]。临床数据显示,24.2%~47.4%的肥胖患者存在食物成瘾
[23-24],其摄食后奖赏相关脑区(如岛叶、眶额皮层)激活强度升高,且与BMI呈正相关
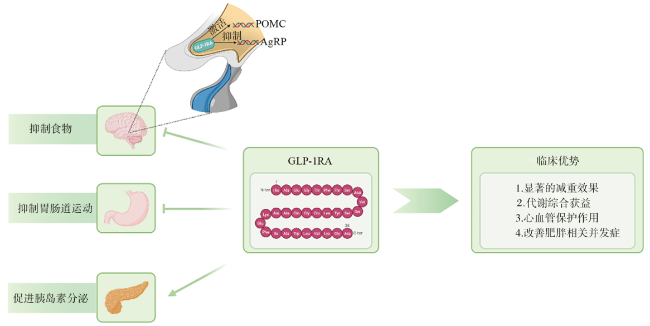
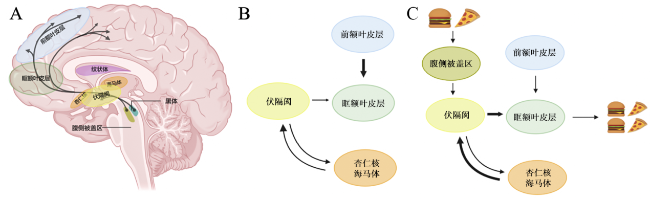
[25-26]。近年研究显示,GLP-1RA可通过多靶点干预这一病理过程,如通过激活下丘脑GLP-1受体(glucagon-like peptide 1 receptor,GLP-1R)抑制刺豚鼠相关肽(agouti-related protein,AgRP)神经元活性,从而降低饥饿感与对高热量食物的奖赏预期
[27]。在动物实验中,研究者通过向大鼠伏隔核注射GLP-1RA,证实了其能够减少伏隔核多巴胺释放,进而削弱甜食诱导的进食快感
[28]。此外,GLP-1RA通过延缓胃排空、促进胆囊收缩素分泌,阻断迷走神经向中枢传递的进食激励信号
[29]。进一步临床研究证实,GLP-1RA治疗可使肥胖患者对高脂/高糖食物的主动回避率提升2~3倍,YFAS评分改善率达65%以上
[30],提示其不仅能调节代谢,更能从神经奖赏层面重塑进食行为模式。