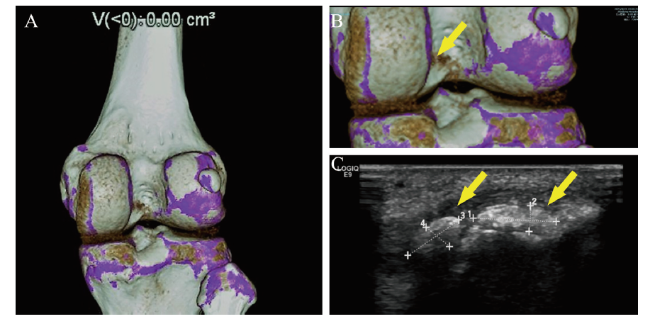
DECT和MSUS作为不同的检查手段,对于GA具有各自的影像学显影特点,在诊断痛风方面各有优势
[11]。MSUS检查提示关节内点状强回声及痛风石是尿酸盐结晶沉积的常见表现,关节腔内暴雪征和双轨征是痛风特征性的超声表现,具有诊断价值
[12⇓-14]。DECT则通过特殊的绿色显影,特异性区分组织与关节周围尿酸盐结晶,更直观地反映尿酸沉积的部位及沉积量。本研究中,65%急性GA患者的DECT未见尿酸盐结晶,而MSUS可显示尿酸盐结晶。MSUS显示尿酸盐总沉积率占88%,其中双轨征占42%,点状结晶及痛风石分别为40%和29%,研究结果符合急性GA首次发作时为疾病早期,具有尿酸盐结晶沉积量相对较少的临床特点,超声影像多显示为点状回声及双轨征,未发现GA反复发作后关节腔内大量尿酸盐漂浮的暴雪征及长期GA发作对骨骼的破坏,而部分超声显示出痛风石的影像可能与长期无症状高尿酸血症相关。由于急性GA首次发作时关节内尿酸盐结晶微量,DECT尚无法显示,因此阳性率低于MSUS。严青等
[15]研究提示,GA患者的双轨征检出率和痛风发生率与血尿酸水平较高相关,与尿酸盐结晶反复析出、沉积有关。Sun等
[16]研究表明,血尿酸水平的升高是双轨征的危险因素。多项研究证实,MSUS可以发现无症状高尿酸血症关节腔内的尿酸盐沉积,表明关节腔在急性炎症发作前已经积累了一定量的尿酸盐结晶。Zhang等
[17]提出,超声应成为GA的首选检查方法,尤其在疾病早期。本研究表明,MSUS对急性GA首次发作患者尿酸盐结晶的检出率高于DECT,且能同时检出关节腔积液、滑膜增生及滑膜炎,因此笔者认为MSUS对于急性GA首次发作的患者可提供更多的信息。